In een nieuw gefinancierd OTP NOW project werkt Stamatialis, verbonden aan het TechMed Centre op de UT, samen met het UMC Utrecht en de universiteiten Utrecht en Maastricht aan het optimaliseren en valideren van een opgeschaalde bio-kunstnier.
Sterfte is vrij hoog
In Nederland hebben duizenden nierpatiënten wekelijkse dialyse nodig. Tijdens deze behandeling wordt het bloed van de patiënt gefilterd door membranen die giftige afvalstoffen, zoals ureum en creatinine, afkomstig van de stofwisseling van het lichaam, verwijderen. ‘Gewoonlijk heeft een patiënt drie keer per week gedurende vier uur dialyse nodig in het ziekenhuis’, zegt Stamatialis. ‘De therapie houdt patiënten in leven totdat er een niertransplantatie beschikbaar is, maar is verre van perfect. De sterfte onder patiënten is vrij hoog en hun kwaliteit van leven is laag.’
Dit komt door de beperkte verwijdering van gifstoffen: dialyse verwijdert minder dan tien procent in vergelijking met een gezonde nier. Vooral de grotere toxines en diegenen die gebonden zijn aan eiwitten worden nauwelijks verwijderd. ‘Bovendien verkeert de patiënt in een constante staat van ontsteking’, zegt Stamatialis. ‘Dit maakt hen erg kwetsbaar voor andere infecties, zoals COVID en hartziekten.’
‘Dialyse is een dure therapie, die ongeveer 100.000 euro per patiënt per jaar kost’
Naast giftige afvalstoffen verwijdert dialyse ook waardevolle moleculen, zoals calcium en kalium. En omdat een zieke nier niet voldoende vitamine D hormonen voor het reguleren van de bloeddruk en belangrijke eiwitten die betrokken zijn bij de synthese van rode bloedcellen kan produceren, moeten deze patiënten dagelijks supplementen krijgen om dit te compenseren. Naast deze onvolkomenheden is dialyse een dure therapie, die ongeveer 100.000 euro per patiënt per jaar kost. Bovendien is de therapie niet bepaald milieuvriendelijk, omdat er ongeveer 400 liter water en enkele kilo's wegwerpplastic nodig is.
Meerdere stappen
In tegenstelling tot de huidige dialysebehandelingen, die het bloed in één stap filteren, doet een gezonde nier dit in meerdere stappen. De twee menselijke nieren verwijderen afvalstoffen van het lichaam door 60 liter bloed per uur te filteren. Elke nier bestaat uit ongeveer een miljoen microscopische filtereenheden, de zogenaamde nefronen. Elk nefron bevat op zijn beurt een glomerulus en een zogenaamde proximale tubulus. De glomerulus filtert voornamelijk water en kleine moleculen uit het bloed, inclusief waardevolle stoffen, zoals glucose, aminozuren, calcium en kalium. Deze stoffen komen vervolgens van de glomerulus in de proximale tubulus. Gespecialiseerde cellen in de wanden van de proximale tubulus re-absorberen water en waardevolle bestanddelen, waardoor deze moleculen niet verloren gaan. Naast reabsorptie verwijderen de proximale tubulus cellen ook grotere en eiwitgebonden gifstoffen.
Enorme verbetering
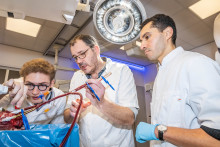
Stamatialis wil nierdialyse stap voor stap verbeteren, met als uiteindelijk doel een implanteerbaar apparaat dat de functie van een gezonde nier nabootst. Hij heeft een eerste belangrijke stap gezet met het verbeteren van de dialysemembranen. In het lab laat hij het nieuwste, geavanceerde membraan zien dat hij en zijn team hebben ontwikkeld. ‘Dit is ons nieuwe M3-membraan, een nieuw ontwerp van een bloedfilter dat meer gifstoffen verwijdert dan de conventionele dialysefilters’, zegt hij.
(Tekst gaat verder onder de foto.)

Hij houdt een 20-centimeter grote cilindervormige plastic kamer vast, een zogenaamde dialyser, met daarin honderden dunne, zwarte, holle vezelmembranen van minder dan een millimeter dik. Het vezelmembraan is uniek: het combineert filtratie en adsorptie en bestaat uit twee lagen: de dunne, witte binnenkant is half poreus en filtert het bloed door gifstoffen door te laten, terwijl het de belangrijkste verbindingen, zoals eiwitten, tegenhoudt. Een tweede, zwarte poreuze laag bevat adsorberende koolstofdeeltjes die zijn ingebed in een polymeermatrix.
‘Om dit nieuwe membraan op de markt te brengen, hebben we steun nodig van investeerders en bedrijven’
Dit deel van het fibermembraan verbetert de bloedzuivering door de gifstoffen te absorberen. Het kan zo eiwitgebonden gifstoffen, die bij conventionele dialyse in het bloed blijven, vrij goed verwijderen. ‘Dit is een enorme verbetering’, zegt Stamatialis. ‘Maar om dit nieuwe membraan op de markt te brengen, hebben we steun nodig van investeerders en bedrijven, bijvoorbeeld dialyse- en polymeerbedrijven, en uiteindelijk moeten we overgaan tot klinische studies. We ontwikkelen ook een eigen spin-off bedrijf om ons M3 membraan op de markt te brengen.’
Bio-artificiële nier
Maar het verbeterde M3 membraan is slechts de eerste stap. Stamatialis' ambities om de dialysetherapie te verbeteren gaan nog verder. In de volgende stap, geïnspireerd door de gezonde nier, wil hij het M3-filter combineren met een zogenaamde bio-artificiële kunstnier (BAK) die bestaat uit levende cellen uit de proximale tubulus van de nier, gekweekt op polymere holle vezelmembranen. ‘Deze cellen zijn in staat om water en waardevolle moleculen opnieuw op te nemen, maar kunnen ook extra gifstoffen verwijderen’, legt hij uit. ‘Als we de BAK kunnen combineren met het M3-membraan in een klein apparaat, kunnen we misschien een implanteerbaar apparaat leveren dat 24/7 meer gifstoffen kan verwijderen. Dit zou een completere behandeling bieden en een algehele betere kwaliteit van leven voor de patiënt.’
Verbeterde functionaliteit
Aangezien er in een echte nier meer filtratiestappen zijn, is het huidige BAK-ontwerp een verbetering, maar nog steeds ver verwijderd van een echte nier. ‘Om de natuurlijke nierfunctie nog beter na te bootsen, kunnen in de toekomst meer compartimenten met verschillende niercellen met verschillende functies worden toegevoegd’, zegt Stamatialis. ‘Als we een verbeterde functionaliteit willen, moeten we dus meer verschillende typen niercellen inbouwen in een toekomstige BAK.’ Om uiteindelijk een complete oplossing te bieden en ziekenhuisbezoeken en kosten te verminderen, moeten wetenschappers zo'n apparaat bij een patiënt implanteren.
Leven dialysepatiënten verbeteren
Om dit te bereiken, moeten ze niet alleen de natuurlijke nier zo goed mogelijk nabootsen, maar ook klein genoeg maken zodat die kan worden geïmplanteerd. Als de wetenschappers al deze stappen kunnen combineren in één apparaat, zijn ze heel dicht bij een bio-artificiële nier die bijna net zo goed functioneert als een echte. Het kan echter nog tientallen jaren duren voordat het zover is. Maar Stamatialis' systematische en stapsgewijze aanpak zou ondertussen geleidelijk het leven van dialysepatiënten kunnen verbeteren, te beginnen met het M3 membraan.
TechMed
Om de M3 membranen op te schalen werkt Stamatialis samen met verschillende onderzoekers op het gebied van kunstmatige organen binnen het Biomed 4 project, van het NXTGEN HighTech groeifonds programma. Zowel de ontwikkeling van de M3 dialyzer als het BAKtothefuture project maken deel uit van het TechMed strategische impulsprogramma KETs4PM over 'Personalised Renal Health' dat als doel heeft een technologische impuls te geven aan de transformatie van gezondheidszorg en welzijn.